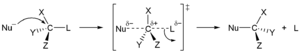Beragamnya reaksi-reaksi kimia dan pendekatan-pendekatan yang dilakukan dalam mempelajarinya mengakibatkan banyaknya cara untuk mengklasifikasikan reaksi-reaksi tersebut, yang sering kali tumpang tindih. Di bawah ini adalah contoh-contoh klasifikasi reaksi kimia yang biasanya digunakan.
[sunting]Empat reaksi dasar
Dalam reaksi
kombinasi langsung atau
sintesis, dua atau lebih senyawa sederhana bergabung membentuk senyawa baru yang lebih kompleks. Dua reaktan atau lebih yang bereaksi menghasilkan satu produk juga merupakan salah satu cara untuk mengetahui kalau itu reaksi sintesis. Contoh dari reaksi ini adalah gas hidrogen bergabung dengan gas oksigen yang hasilnya adalah air.
[15]Contoh lainnya adalah gas nitrogen bergabung dengan gas hidrogen akan membentuk amoniak, dengan persamaan reaksi:
- N2 + 3 H2 → 2 NH3
[sunting]Dekomposisisi
Reaksi
dekomposisi atau
analisis adalah kebalikan dari reaksi sintesis. Sebuah senyawa yang lebih kompleks akan dipecah menjadi senyawa yang lebih sederhana.
[15][16] Contohnya adalah molekul air yang dipecah menjadi gas oksigen dan gas hidrogen, dengan persamaan reaksi:
- 2 H2O → 2 H2 + O2
[sunting]Penggantian tunggal
Dalam
reaksi penggantian tunggal atau
substitusi, sebuah elemen tunggal menggantikan elemen tunggal lainnya di suatu senyawa. Contohnya adalah logam natrium yang bereaksi dengan asam klorida akan menghasilkan
natrium klorida atau garam dapur, dengan persamaaan reaksi:
- 2 Na(s) + 2 HCl(aq) → 2 NaCl(aq) + H2(g)
[sunting]Penggantian ganda
Dalam reaksi penggantian ganda, dua senyawa saling berganti
ion atau ikatan untuk membentuk senyawa baru yang berbeda.
[15] Hal ini terjadi ketika kation dan anion dari 2 senyawa yang berbeda saling berpindah tempat, dan membentuk 2 senyawa baru.
[16] Rumus umum dari reaksi ini adalah:
- AB + CD → AD + CB
Contoh dari reaksi penggantian ganda adalah timbal(II) nitrat bereaksi dengan kalium iodida untuk membentuk timbal(II) iodida dan kalium nitrat, dengan persamaan reaksi:
- Pb(NO3)2 + 2 KI → PbI2 + 2 KNO3
Contoh lainnya adalah natrium klorida (garam dapur) bereaksi dengan perak nitrat membentuk natrium nitrat dan perak klorida, dengan persamaan reaksi:
- NaCl(aq) + AgNO3(aq) → NaNO3(aq) + AgCl(s)
[sunting]Oksidasi dan reduksi
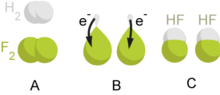
Ilustrasi dari reaksi redoks (reduksi oksidasi)
Reaksi
redoks dapat dipahami sebagai transfer elektron dari salah satu senyawa (disebut
reduktor) ke senyawa lainnya (disebut
oksidator). Dalam proses ini, senyawa yang satu akan teroksidasi dan senyawa lainnya akan tereduksi, oleh karena itu disebut
redoks. Oksidasi sendiri dimengerti sebagai kenaikan
bilangan oksidasi, dan reduksi adalah penurunan
bilangan oksidasi. Dalam prakteknya, transfer dari elektron ini akan selalu mengubah bilangan oksidasinya, tapi banyak reaksi yang diklasifikasikan sebagai reaksi redoks walaupun sebenarnya tidak ada elektron yang berpindah (seperti yang melibatkan ikatan
kovalen).
[17][18]Contoh reaksi redoks adalah:
- 2 S2O32−(aq) + I2(aq) → S4O62−(aq) + 2 I−(aq)
- Yang mana I2 direduksi menjadi I- dan S2O32- (anion tiosulfat) dioksidasi menjadi S4O62-.
Untuk mengetahui reaktan mana yang akan menjadi agen pereduksi dan mana yang akan menjadi agen teroksidasi dapat diketahui dari
keelektronegatifanelemen tersebut. Elemen yang mempunyai nilai keelektronegatifan yang rendah, seperti kebanyakan unsur
logam, maka akan dengan mudah memberikan elektron mereka dan teroksidasi - elemen ini menjadi reduktor. Kebalikannya, banyak ion mempunyai bilangan oksidasi tinggi, seperti
H2O2,
MnO4-,
CrO3,
Cr2O72-,
OsO4) dapat memperoleh satu atau lebih tambahan elektron, sehingga disebut oksidator.
Jumlah elektron yang diberikan atau diterima pada reaksi redoks dapat diketahui dari
konfigurasi elektronn elemen reaktannya. Setiap elemen akan berusaha untuk menjadikan konfigurasi elektronnya sama seperti konfigurasi elemen
gas mulia. Logam alkali dan halogen akan memberikan dan menerima satu elektron. Elemen gas alam sendiri sebenarnya tidak aktif secara kimiawi.
[19]Salah satu bagian penting dalam reaksi redoks adalah reaksi
elektrokimia, dimana elektron dari sumber listrik digunakan sebagai reduktor. Reaksi ini penting untuk pembuatan elemen-elemen kimia, seperti
klorin[20] atau
aluminium. Proses kebalikan dimana reaksi redoks digunakan untuk menghasilkan listrik juga ada dan prinsip ini digunakan pada
baterai.
[sunting]Reaksi asam-basa
Reaksi asam-basa adalah reaksi yang mendonorkan proton dari sebuah molekul
asam ke molekul
basa. Disini,
asam berperan sebagai donor proton dan
basa berperan sebagai akseptor proton.

- Reaksi asam basa, HA: asam, B: Basa, A–: basa konjugasi, HB+: asam konjugasi
Hasil dari transfer proton ini adalah
asam konjugasi dan
basa konjugasi.
[21] Reaksi kesetimbangan (bolak-balik) juga ada, dan karena itu asam/basa dan asam/basa konjugasinya selalu dalam kesetimbangan. Reaksi kesetimbangan ini ditandai dengan adanya
konstanta diasosiasi asam dan basa (
Ka dan
Kb) dari setiap substansinya. Sebuah reaksi yang khusus dari reaksi asam-basa adalah
netralisasi dimana asam dan basa dalam jumlah yang sama akan membentuk
garam yang sifatnya netral.
Reaksi asam basa memiliki berbagai definisi tergantung pada konsep asam basa yang digunakan. Beberapa definisi yang paling umum adalah:
- Definisi Arrhenius: asam berdisosiasi dalam air melepaskan ion H3O+; basa berdisosiasi dalam air melepaskan ion OH-.
- Definisi Brønsted-Lowry: Asam adalah pendonor proton (H+) donors; basa adalah penerima (akseptor) proton. Melingkupi definisi Arrhenius
- Definisi Lewis: Asam adalah akseptor pasangan elektron; basa adalah pendonor pasangan elektron. Definisi ini melingkupi definisi Brønsted-Lowry.
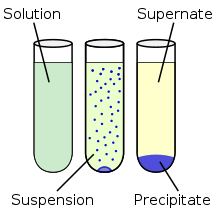
Presipitasi adalah proses reaksi terbentuknya padatan (endapan) di dalam sebuah larutan sebagai hasil dari reaksi kimia. Presipitasi ini biasanya terbentuk ketika konsentrasi ion yang larut telah mencapai batas
kelarutan[22] dan hasilnya adalah membentuk
garam. Reaksi ini dapat dipercepat dengan menambahkan agen presipitasi atau mengurangi pelarutnya. Reaksi presipitasi yang cepat akan menghasilkan residu mikrokristalin dan proses yang lambat akan menghasilkan
kristal tunggal. Kristal tunggal juga dapat diperoleh dari
rekristalisasi dari garam mikrokristalin.
[23] [sunting]Reaksi pada zat padat
Reaksi dapat terjadi diantara dua benda padat. Meski begitu, karena tingkat
difusi pada zat padat sangat rendah, maka reaksi kimia yang berlangsung terjadi sangat lambat. Reaksi dapat dipercepat dengan cara meningkatkan suhu sehingga akan memecah reaktan, sehingga luas permukaan kontak menjadi lebih besar.
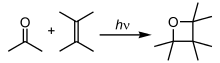
[24][sunting]Reaksi fotokimia

Diagram skema energi yang menunjukkan efek dari pemberian katalis pada sebuah reaksi kimia endotermik. Adanya katalis akan mempercepat reaksi dengan cara menurunkan energi aktivasi. Hasil akhirnya akan sama dengan reaksi tanpa katalis.
Pada
katalisis, reaksinya tidak berlangsung secara spontan, tapi melalui substansi ketiga yang disebut dengan
katalis. Tidak seperti reagen lainnya yang ikut dalam reaksi kimia, katalis tidak ikut serta dalam reaksi itu sendiri, tapi dapat menghambat, mematikan, atau menghancurkan melalui proses sekunder. Katalis dapat digunakan pada fase yang berbeda (
katalis heterogen) maupun pada fase yang sama (
katalis homogen) sebagai reaktan. Fungsi katalis hanyalah mempercepat reaksi - zat kimia yang memperlambat reaksi disebut dengan inhibitor.
[27][28] Substansi yang meningkatkan aktivitas katalis disebut promoter, dan substansi yang mematikan katalis disebut racun katalis. Sebuah reaksi kimia yang semestinya tidak bisa berlangsung karena energi aktivasinya terlalu tinggi, bisa menjadi berlangsung karena kehadiran katalis ini.
Katalis heterogen biasanya padat dan berbentuk bubuk agar dapat memaksimalkan luas permukaan yang bereaksi. Zat-zat yang penting pada katalisis heterogen diantaranya logam-logam
grup platinum dan logam transisi lainnya. Zat-zat ini biasanya digunakan pada
hidrogenasi,
pembentukan katalitik dan sintesis dari senyawa-senyawa kimia seperti
asam nitrat dan
amonia. Asam adalah contoh dari katalis homogen, mereka meningkatkan nukleofilitas dari
karbonil. Kelebihan dari katalis homogen adalah mudah untuk dicampurkan dengan reaktannya, tapi kekurangannya adalah susah dipisahkan dari produk akhirnya. Oleh karena itu, katalis heterogen lebih dipilih di banyak proses industri.
[29][sunting]Reaksi dalam kimia organik
Dalam kimia organik, banyak reaksi yang dapat terjadi yang melibatkan
ikatan kovalen diantara atom karbon dan heteroatom lainnya seperti
oksigen,
nitrogen, atau atom-atom
halogen lainnya. Beberapa reaksi yang lebih spesifik akan dijelaskan di bawah ini.
Pada tipe yang pertama,
nukleofil, atom atau molekul yang memiliki kelebihan elektron sehingga bermuatan negatif, akan menggantikan atom lainnya atau bagian lainnya dari molekul "substrat". Pasangan elektron nukleofil akan bersatu dengan substrat membentuk ikatan baru, sedangkan
gugus lepas akan lepas bersamaan dengan sebuah pasangan elektron. Nukleofil sendiri dapat bermuatan netral atau positif, sedangkan substrat biasanya bermuatan positif atau netral. Contoh nukleofil adalah ion
hidroksida,
alkoksida,
amina, dan
halida. Reaksi semacam ini biasanya ditemukan pada
hidrokarbon alifatik dan jarang ditemukan pada
hidrokarbon aromatik. Hidrokarbon aromatik memiliki rapatan elektron yang tingi dan hanya bisa melangsungkan
substitusi aromatik nukleofilik hanya dengan gugus penarik elektron yang sangat kuat. Substitusi nukleofilik dapat berlangsung melalui 2 mekanisme,
Reaksi SN1 dan
SN2. Menurut namanya, S singkatan dari substitusi, N singkatan dai nukleofilik, dan, dan angka menunjukkan
ordo kinetik reaksi, unimolekuler atau bimolekuler.
[31]3 tahap dalam
Reaksi SN2. Nukleofil berwarna hijau dan gugus lepas berwarna merah
Reaksi SN2 menyebabkan inversi stereo (inversi Walden)
Reaksi S
N1 berlangsung dalam 2 tahap. Tahap pertama,
gugus lepas akan lepas dan membentuk
karbokation. Tahap ini akan diikuti reaksi yang sangat cepat dengan nukleofil.
[32]Dalam mekanisme S
N2, nukleofil akan membentuk tahap transisi dengan molekul yang lepas saja yang terlekang. Kedua mekanisme ini berbeda pada hasil
stereokimianya. Reaksi S
N1 menghasilkan adisi non-stereospesifik dan tidak menghasilkan pusat
chiral, melainkan dalam bentuk
isomer geometri (
cis/trans). Kebalikannya, inversi Warden-lah yang diamati pada mekanisme S
N2.
[33]Substitusi elektrofilik merupakan kebalikan dari substitusi nukleofilik di mana atom atau molekul yang melepas, atau
elektrofilnya, mempunyai kerapatan elektron yang rendah sehingga bermuatan positif. Biasanya elektrofil ini adalah atom karbon dari
gugus karbonil, karbokation atau
sulfur atau kation
nitronium. Reaksi ini berlangsung pada hidrokarbon aromatik saja, sehingga disebut
substitusi aromatik elektrofilik. Serangan elektrofil akan menciptakan kompleks yang disebut sebagai σ-compleks, sebuah fase transisi di mana sistem aromatiknya hilang. Lalu, gugus lepas (biasanya proton), akan terpisah dan sifat kearomatikannya kembali. Alternatif lain untuk substitusi aromatik adalah substitusi alifatik elektrofilik. Substitusi ini mirip dengan substitusi aromatik elektrofilik dan juga mempunyai 2 tipe utama yaitu S
E1 dan S
E2
[34] 
Mekanisme dari substitusi aromatik elektrofilik
[sunting]Adisi dan eliminasi
Adisi dan pasangannya
eliminasi merupakan reaksi yang mengubah jumlah substituen dalam atom karbon, dan membentuk
ikatan kovalen.
Ikatan ganda dan
tiga dapat dihasilkan dengan mengeliminasi gugus lepas yang cocok. Seperti substitusi nukleofilik, ada beberapa mekanisme reaksi yang mungkin terjadi. Dalam mekanisme E1, gugus lepas terlebih dahulu melepas dan membentuk karbokation. Selanjutnya, pembentukan ikatan ganda terjadi melalui eliminasi proton (
deprotonasi). Dalam mekanisme E1cb, urutan pelepasan terbalik: proton dieliminasi terlebih dahulu. Dalam mekanisme ini keterlibatan suatu basa harus ada.
[35] Reaksi dalam eliminasi E1 maupun E1cb selalu bersaing dengan substitusi S
N1 karena memiliki kondisi reaksi kondisi yang sama.
[36]
 | |  |
Eliminasi E1 | | eliminasi E1cb |
Mekanisme E2 juga memerlukan basa. Akan tetapi, pergantian posisi basa dan eliminasi gugus lepas berlangsung secara serentak dan tidak menghasilkan zat antara ionik. Berbeda dengan eliminasi E1, konfigurasi stereokimia yang berbeda dapat dihasilkan dalam reaksi yang memiliki mekanisme E2 karena basa akan lebih memfavoritkan eleminasi proton yang berada pada posisi-anti terhadap gugus lepas. Oleh karena kondisi dan reagen reaksi yang mirip, eliminasi E2 selalu bersaing dengan substitusi S
N2.
[37]
Adisi elektrofilik hidrogen bromida
Kebalikan dari reaksi eliminasi adalah reaksi adisi. Pada reaksi adisi, ikatan rangkap dua atau rangkap tiga diubah menjadi ikatan rangkap tunggal. Mirip dengan reaksi substitusi, ada beberapa tipe dari adisi yang dibedakan dari partikel yang mengadisi. Contohnya, pada
adisi elektrofilik hidrogen bromida, sebuah elektrofil (proton) akan mengganti ikatan rangkap ganda dan membentuk
karbokation, lalu kemudian bereaksi dengan nukleofil (bromin). Karbokation dapat terbentuk di salah satu ikatan rangkap tergantung dari gugus yang melekat di akhir. Konfigurasi yang lebih tepat dapat diprediksikan dengan
aturan Markovnikov.
[38] Aturan Markovnikov mengatakan: "Pada adisi heterolitik dari sebuuah molekul polar pada alkena atau alkuna, atom yang mempunyai keelektronegatifan yang besar, maka akan terikat pada atom karbon yang mengikat atom hidrogen yang lebih sedikit."
[39][sunting]Reaksi kimia organik lainnya

Penataan ulang dari 3-metil-1,5-heksadiena
Mekanisme dari reaksi Diels-Alder
Orbital overlap in a Diels-Alder reaction
[sunting]Reaksi lainnya
- Isomerisasi, yang mana senyawa kimia menjalani penataan ulang struktur tanpa perubahan pada komposisi atomnya
- Pembakaran, adalah sejenis reaksi redoks yang mana bahan-bahan yang dapat terbakar bergabung dengan unsur-unsur oksidator, biasanya oksigen, untuk menghasilkan panas dan membentuk produk yang teroksidasi. Istilah pembakaran biasanya digunakan untuk merujuk hanya pada oksidasi skala besar pada keseluruhan molekul. Oksidasi terkontrol hanya pada satu gugus fungsi tunggal tidak termasuk dalam proses pembakaran.
- C10H8+ 12 O2 → 10 CO2 + 4 H2O
- CH2S + 6 F2 → CF4 + 2 HF + SF6
- Disproporsionasi, dengan satu reaktan membentuk dua jenis produk yang berbeda hanya pada keadaan oksidasinya.
- 2 Sn2+ → Sn + Sn4+
[sunting]Kinetika kimia
Laju reaksi suatu reaksi kimia merupakan pengukuran bagaimana
konsentrasi ataupun
tekanan zat-zat yang terlibat dalam reaksi berubah seiring dengan berjalannya waktu. Analisis laju reaksi sangatlah penting dan memiliki banyak kegunaan, misalnya dalam
teknik kimia dan kajian
kesetimbangan kimia. Laju reaksi secara mendasar tergantung pada:
- Konsentrasi reaktan, yang biasanya membuat reaksi berjalan dengan lebih cepat apabila konsentrasinya dinaikkan. Hal ini diakibatkan karena peningkatan pertumbukan atom per satuan waktu,
- Luas permukaan yang tersedia bagi reaktan untuk saling berinteraksi, terutama reaktan padat dalam sistem heterogen. Luas permukaan yang besar akan meningkatkan laju reaksi.
- Tekanan, dengan meningkatkan tekanan, kita menurunkan volume antar molekul sehingga akan meningkatkan frekuensi tumbukan molekul.
- Energi aktivasi, yang didefinisikan sebagai jumlah energi yang diperlukan untuk membuat reaksi bermulai dan berjalan secara spontan. Energi aktivasi yang lebih tinggi mengimplikasikan bahwa reaktan memerlukan lebih banyak energi untuk memulai reaksi daripada reaksi yang berenergi aktivasi lebih rendah.
- Temperatur, yang meningkatkan laju reaksi apabila dinaikkan, hal ini dikarenakan temperatur yang tinggi meningkatkan energi molekul, sehingga meningkatkan tumbukan antar molekul per satuan waktu.
- Keberadaan ataupun ketiadaan katalis. Katalis adalah zat yang mengubah lintasan (mekanisme) suatu reaksi dan akan meningkatkan laju reaksi dengan menurunkan energi aktivasi yang diperlukan agar reaksi dapat berjalan. Katalis tidak dikonsumsi ataupun berubah selama reaksi, sehingga ia dapat digunakan kembali.
- Untuk beberapa reaksi, keberadaan radiasi elektromagnetik, utamanya ultraviolet, diperlukan untuk memutuskan ikatan yang diperlukan agar reaksi dapat bermulai. Hal ini utamanya terjadi pada reaksi yang melibatkan radikal.
Laju reaksi berhubungan dengan
konsentrasi zat-zat yang terlibat dalam reaksi. Hubungan ini ditentukan oleh
persamaan laju tiap-tiap reaksi. Perlu diperhatikan bahwa beberapa reaksi memiliki kelajuan yang
tidak tergantung pada konsentrasi reaksi. Hal ini disebut sebagai reaksi orde nol.
[sunting]Reaksi biokimia
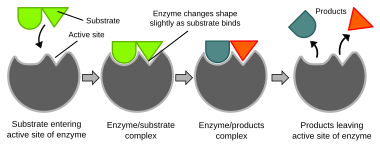
Ilustrasi dari aktivitas enzim pada reaksi biokimia
Reaksi biokimia pada umumnya dikendalikan oleh
enzim.
Protein-protein ini hanya dapat
mengkatalis satu jenis reaksi yang spesifik, sehingga reaksinya benar-benar dapat dikontrol. Reaksi ini berlangsung pada
sisi aktif dari substrat. Reaksi katalisasi enzim ini bergantung pada banyak hal, diantaranya adalah bentuk enzimnya, jenis ikatannya, interaksi elektrostatik, pemberian dan penerimaan proton (pada reaksi asam/basa), dan lainnya.
[41] Reaksi kimia yang berlangsung di dalam tubuh makhluk hidup biasanya juga dikenal dengan sebutan
metabolisme. Diantara semua reaksi-reaksi ini, reaksi yang paling penting adalah reaksi
anabolisme, dimana
DNA dan enzim-terkontrol memproses pembentukan
protein dan
karbohidrat dari senyawa-senyawa yang lebih kecil.
[42] Bioenergitika mempelajari sumber energi untuk reaksi biokimia. Sumber energi yang paling penting dalam reaksi ini adalah
glukosa, yang diproduksi tanaman melalui proses
fotosintesis. Semua organisme membutuhkan glukosa untuk memproduksi
adenosin trifosfat (ATP), yang digunakan makhluk hidup untuk menjalankan aktivitasnya.
[sunting]Penggunaan reaksi kimia

Reaksi termit digunakan dalam proses pengelasan.
Reaksi kimia sangat sering digunakan oleh para ahli
teknik kimia untuk mensintesis senyawa baru dari sumber daya alam mentah di alam, seperti
minyak bumi dan bijih-bijih mineral. Merupakan suatu hal yang penting untuk membuat reaksi yang seefisien mungkin, memaksimalkan hasil yang bisa diperoleh dan meminimalkan reagen yang dipakai, energi masuk dan energi keluar.
Katalis biasanya digunakan untuk mengurangi energi aktivasi sehingga meningkatkan laju reaksinya.
[43][44]Beberapa reaksi yang spesifik mempunyai penggunaan yang khusus. Misalnya, reaksi
termit dipakai untuk menghasilkan cahaya dan panas pada
piroteknikdan
pengelasan. Meskipun reaksi ini lebih agak sulit dikontrol daripada reakai-reaksi sebelumnua, tapi alat-alat yang dibutuhkan jauh lebih sedikit dan sampai saat ini masih digunakan untuk memperbaiki jalur-jalur kereta api di tempat-tempat terpelosok.
[45]